- 1
- *
 20. decembar 2009.
20. decembar 2009.
Hemija
Izvor: www.nobelprize.org
Preveo: S. Milovanović
Ključ života na atomskom nivou
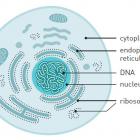
Na početku dvadesetog veka, hemijske osnove života bile su velika tajna. Danas znamo kako veliki broj važnih životnih procesa funkcioniše čak i na atomskom nivou. Nobelova nagrada za hemiju u 2009. godini dodeljena je za detaljno mapiranje ribozoma – organela koje predstavljaju pravu ćelijsku fabriku proteina. Ribozomi prevode pasivne DNK informacije u formu i funkciju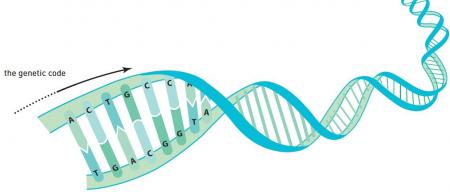
Opšta teorija evolucije koju je objavio Čarls Darvin 1859. godine, zasnovana je na pretpostavci da su osobine organizama nasledne i da se ponekad događaju nasumične promene. Uspešne promene koje povećavaju šansu za preživljavanje organizma prenose se dalje, na buduće generacije.
Kada je naučna zajednica razumela Darvinove stavove, pojavila su se nova pitanja: šta se tačno prenosi između generacija, gde se pojavljuju nasumične promene i kako se one odlikuju u živom organizmu?
Nobelova nagrada za hemiju 2009. godine, treća je u nizu nagrada koje pokazuju, na nivou atoma, kako Darvinove teorije zaista funkcionišu. Slike nastale raznim tehnikama rendgenske strukturne analize (kristalografije), pokazuju kako se prost DNK kod može ispoljiti, ne samo kao sluh, osećaj i ukus, ili mišić, kost i koža, već i kao misli ili govor.
Trilogija nagrada je počela sa jednom od najčuvenijih Nobelovih nagrada ikada, kada su Džejms Votson (James Watson), Frensis Krik (Francis Crick) i Mauris Vilkins (Maurice Wilkins) nagrađeni za usavršenje atomskog modela dvolančanog DNK molekula, 1962. godine. Druga nagrada u pomenutoj trilogiji dodeljena je 2006. godine Rodžeru Kornbergu (Roger Kornberg) za rendgenske strukture koje objašnjavaju kako se informacije kopiraju na informacioni RNK molekul.
Ribozom prevodi genetsku informaciju u aktivnost
Tri nosioca Nobelove nagrade za hemiju u 2009. godini, Ada Jonat (Ada Yonath), Tomas Steic (Thomas Steitz) i Venkatraman Ramakrišnan (Venkatraman Ramakrishnan), nagrađeni su za mapiranje ribozoma, jednog od najkompleksnijih ćelijskih aparata, na atomskom nivou. Ribozom čita informacije iz informacione RNK i na osnovu te informacije proizvodi odgovarajući protein. Naučnici ovu pojavu često zovu prevođenjem. Upravo tokom ovog prevodilačkog procesa, kada DNK/RNK jezik postaje jezik proteina, život dostiže svoju punu kompleksnost.
Živi organizam sadrži desetine hiljada različitih proteina koji kontrolišu procese u telu sa zapanjujućom preciznošću. Primeri takvih proteina su: hemoglobin, koji prenosi kiseonik od pluća do ostatka tela; insulin, koji kontroliše nivo šećera u krvi; antitela koja zarobljavaju viruse i keratin, od kojeg su sačinjeni kosa i nokti.
Ribozomi postoje u svim ćelijama živih organizama, od bakterija pa do ljudskih bića. Kako nijedno živo stvorenje ne može da preživi bez ribozoma, oni su savršene mete za lekove. Veliki broj današnjih antibiotika napadaju ribozome bakterija, ali ne dirajući one ljudske. Znanje koje su nam ovogodišnji Nobelovi laureati predstavili, može biti od ogromne važnosti za razvoj novih antibiotika.
Proteini – „nizovi amino kiselinskih kuglica“
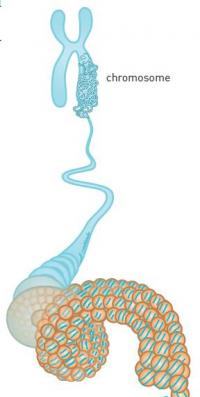
Početkom četrdesetih godina prošlog veka, mapiranje ćelije je napredovalo do takve mere, da su naučnici tada već znali da se nasledne osobine prenose pomoću hromozoma. Hromozomi se sastoje od nukleinskih kiselina (DNK) i proteina. Većina naučne zajednice mislila je da su proteini nosioci naslednih osobina zbog toga što su kompleksniji od DNK.
Naučnici su bili fascinirani proteinima. Bilo je poznato da neki proteini funkcionišu kao gradivni materijal, dok drugi, kao što su enzimi, aktiviraju i kontrolišu hemijske reakcije. Međutim, iako oni igraju toliko različitih uloga u ćeliji, svi proteini se sastoje od istih gradivnih blokova, tačnije 20 različitih vrsta amino kiselina. Kao nanizane kuglice, oni su povezani dugačkim lancima. Njihova veza, poznata kao peptidna veza, veoma je stabilna. Proteinski lanac se može sastojati od 10 pa do 10 000 amino kiselina. Insulin, primera radi, mnogo je kraći od hemoglobina.
DNK molekul – previše prost da bi bio prenosilac naslednih osobina?
DNK molekul je bio od malog interesa za naučnike četrdesetih godina prošlog veka. Godine 1871. Fridrih Miešer (Friedrich Miescher), švajcarski naučnik, bio je prvi koji je izolovao DNK molekul iz nukleusa ćelije. On je imenovao novootkriveni molekul, nuklein.
Slično kao i proteini, DNK molekululi se sastoje od nizova kuglica manjih molekula. DNK, međutim, sastoji se samo od četiri različite „kuglice“ – nukleotida. Oni predstavljaju nosioce četiri hemijske grupe: adenin (A), citozin (C), guanin (G) i timin (T).
Samo četiri gradivna bloka izgledala su kao premali broj da bi se izveo bilo kakav važan zadatak u ćeliji. Stoga se verovalo da je DNK uglavnom služila kao skelet za proteine hromozoma.
Ipak, 1944. je bila godina povratka DNK molekula. U onome što je poznato kao Averi-Makliod-Mekarti (Avery-MacLeod-McCarty) eksperiment, DNK mrtvih bakterija ubačena je u žive bakterije. Rezultat je bio da su se one promenile i postale zarazne (izazivači bolesti). Dok je eksperiment bio kritikovan, DNK je postala novi fokus pažnje naučne zajednice. Razumevanje kako DNK može prenositi nasledne osobine je dosegnuto sa otkrivanjem atomskog modela dvostruke helikoide.
Njeno veličanstvo: dvostruka helikoida
28. februara 1953. godine, Džejms Votson (James Watson) i Frensis Krik (Francis Crick) u Kevendiš laboratoriji, na Univerzitetu Kembridž u Velikoj Britaniji, spojili su delove DNK slagalice. Nekoliko godina su oni pokušavali da reše kako bi se četiri nukleotida DNK molekula mogla sastaviti u trodimenzionalnu strukturu.
Čista i oštra rendgenska difrakciona slika, koju je napravila Rozalind Frenklin (Rosalind Franklin), pokazala je, pored raznih stvari, da DNK formira prostornu spiralu - helikoidu, koja se sastoji iz dve niti. Analize biohemičara Ervina Čargafa (Erwin Chargaff) pokazale su da DNK, bilo da potiče od bakterije, insekta ili životinje, uvek sadrži istu količinu adenina (A) i timina (T), kao i istu količinu citozina (C) i guanina (G).
Votson i Krik, međutim, su radili sa pogrešnim hemijskim formulama nukleotida. Korekcija kolege je dovela do njihovog saznanja da se A povezuje sa T, a G sa C. Nukleotidni parovi, poznatiji kao osnovni parovi, imaju istu veličinu i savršeno se uklapaju u dvostruku spiralu.
Naučna zajednica je ubrzo shvatila da je genetski kod sadržan u nukleotidnim serijama svakog od nukleotidnih nizova. ATTGCCAT na primer, predstavlja nešto sasvim drugačije od GCGTATAG. Naučnici su shvatili da redosled nukleotida kontroliše redosled amino kiselina u proteinima. Pitanje koje je ostalo bilo je: Kako?
RNK – rođaka od DNK
U isto vreme dok su Votson i Krik radili na svom velikom otkriću, naučna zajednica postala je sve više i više zainteresovana za drugu nukleinsku kiselinu, koja je pronađena u citoplazmi (delu ćelije van nukleusa). Dugo se znalo da DNK ima rođaku - RNK, koja se takođe sastoji iz četiri različita nukleotida. Umesto timina (T), koji se nalazi u DNK, RNK je sadržala uracil (U).
Početkom pedestih godina prošlog veka, naučnici su znali da se najveći deo RNK nalazi u citoplazmi. Kasnije se otkrilo da je to mesto gde se i proteini proizvode. 1958. godine, nazavli su česticu koja proizvodi proteine ribozom. Ona se sastoji od proteina i RNK molekula (ribozomska RNK ili rRNK).
Genetski kod biva dešifrovan
Dakle, 100 godina nakon što je Darvin razradio svoju teoriju evolucije, naučnici su identifikovali DNK kao molekul koji prenosi nasledne osobine. Niz nukleotida kontroliše redosled amino kiselina u proteinima, koji su proizvedeni od strane ribozoma u citoplazmi. Ali šta je veza između DNK i ribozoma?
Odgovor je pronađen početkom šezdesetih godina. Naučnici su shvatili da je genetska poruka kopirana na RNK molekul. Nazvali su ga informaciona RNK (iRNK). iRNK se kreće van nukleusa i biva uhvaćena od strane ribozoma, koji je koristi kao uputstvo za proizvodnju proteina.
Kada je prethodno postalo poznato, naučnici su ubrzo dešifrovali genetski kod uz pomoć veštačkih iRNK i ribozoma u eksperimentima. Ribozom čita nukleotide u iRNK tripletima ili kodonima. Prvi kodon koji je otkriven je UUU, koji preveden od strane ribozoma predstavlja amino kiselinu fenilanin. Postoje 64 različita kodona i 20 amino kiselina, tako da su neke od amino kiselina kodirane od strane više kodona.
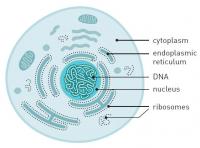
Samo čitanje je omogućeno zahvaljujući drugom RNK molekulu, transportnoj RNK (tRNK). Na jednom kraju tRNK nalazi se antikodon, koji je uparen sa odgovarajućim kodonom na iRNK molekulu u ribozomu. Na drugom kraju, nalazi se specifična amino kiselina koja povezuje kodon.
Tu se pojavila slika najfundamentalnijeg procesa života: način na koji informacija teče od DNK do RNK i nastaju enzimi i drugi proteini. Slika je i dalje bila više šematska. Kako je Votson 1964. godine izjavio u medijima: „Nažalost, mi ne možemo precizno da opišemo na hemijskom nivou kako molekul funkcioniše, a da prethodno ne znamo njegovu strukturu“. Bilo je potrebno vremena sve do 2000. godine da neko napravi model koji je pokazao kako su atomi raspoređeni u ribozomu.
Ada Jonat – pionir snažne volje
Često se dešava da do revolucionarnih otkrića dolaze pioniri koji istražuju nepoznatu teritoriju. U ovom slučaju taj pionir je bila Ada Jonat. Krajem sedamdesetih godina prošlog veka, ona je odlučila da pokuša da generiše rendgenske kristalografske strukture ribozoma. U to vreme većina naučnika je smatrala da je to nemoguće.
Rendgenska kristalografija podrazumeva usmeravanje rendgenskog zračenja u kristal, na primer, proteina. Kada zraci pogode atome kristalne rešetke, oni se rasipaju. Sa druge strane kristala, naučnici očitavaju kako su se zraci rasuli. Ranije se to radilo koristeći fotografski film, koji je bivao zatamljen zračenjem. Danas se koriste CCD detektori (Nobelova nagrada za fiziku 2009. godine), koji se nalaze u modernim digitalnim fotoaparatima. Analizirajući ovako nastale snimke, naučnici mogu precizno odrediti kako su atomi pozicionirani u proteinu.
Međutim, za ovaj proces kristal mora biti skoro savršen, molekuli moraju formirati preciznu formaciju koja se ponavlja iznova i iznova. Uz malo sreće, kada se slana voda pusti da lagano isparava, formiraju se predivni kristali soli, ali ako se pusti da slana voda ključa, so se formira samo na dnu posude i ima nepravilnu strukturu. Dakle, različiti uslovi utiču na formiranje manje ili više korisnih kristala za istraživanje.
U velikoj meri, ovo važi i za kristale za rendgensku strukturnu analizu (kristalografiju). Dobijanje kvalitetnih kristala iz proteina je veoma težak zadatak i što je veći proteinski kompleks, teže je obaviti ovaj posao.
Stoga, mnogo ljudi je bilo skeptično po pitanju vizije Ade Jonat. Ribozom je jedan od najkomplikovanijih protein/RNK komplekasa. Podeljen je u dva dela, malu podjedinicu i veliku podjedinicu. Mala podjedinica ljudskog ribozoma se sastoji od velikog RNK molekula i oko 32 proteina, dok se velika podjedinica sastoji od 3 RNK molekula i oko 46 proteina. Dakle, svaka od podjedinica se sastoji od hiljada nukleotida i amino kiselina, koji se, opet, sastoje od stotina hiljada atoma. Ada Jonat je želela da definiše tačnu lokaciju svakog od ovih atoma u ribozomu.
Topla proleća i Mrtvo more – što suroviji uslovi, to bolji kristal
Kada je Ada Jonat odlučila da kristalizuje ribozom, izabrala je da radi sa bakterijom koja živi u ekstremnim uslovima. Geobacillus stearothermophilus živi tokom toplih proleća i preživljava tempreature do 75 stepeni Celzijusa. Pretpostavka Ade Jonat bila je da ribozom ove bakterije mora biti ekstremno stabilan i stoga bi formirao odgovarajuće kristale.
1980. godine, ona je već uspela da generiše prve trodimenzionalne kristale velike podjedinice ribozoma. Ovo je bilo ogromno dostignuće, iako su kristali bili daleko od savršenih.
Bilo je potrebno još 20 godina napornog rada da bi Ada Jonat mogla da napravi sliku ribozoma takvu da se na njoj može odrediti položaj svakog atoma. Probala je mnogo novih stvari. Pokušavala je da stabilizuje kristale smrzavajući ih u tečnom azotu na temperaturi od -196 stepeni Celzijusa. Takođe je probala da kristalizuje ribozome drugih mikroorganizama. Jedan od njih je bio Haloarcula marismortui koji živi u Mrtvom moru.
Korak po korak, Ada Jonat se približavala cilju. Najzad, shvatilo se da se ribozomska struktura može mapirati i još naučnika se pridružilo trci. Među njima su bili Tomas Steic i Venkatraman Ramakrišnan.
Slika od miliona crnih tačkica sa značenjem
Početkom devedesetih godina prošlog veka, kristali koje je Ada Jonat koristila, imali su dovoljan kvalitet. Slika sačinjena od crnih tačkica je bila dovoljno detaljna za određivanje položaja atoma u kristalu ribozoma. Međutim, postojala je jedna prepreka. To je bio fazni problem rendgenske kristalografije. Da bi se modelirala struktura sa slike od crnih tačaka, naučnici su morali da znaju fazni ugao za svaku tačku. Ova matematička informacija je vezana za lokaciju atoma u kristalu.
Trik koji su naučnici često koristili da bi odredili fazne uglove bio je potapanje kristala u teške atome kao što je živa (Hg). Teški atomi se vežu za površinu kristala ribozoma i onda upoređujući slike kristala sa ili bez teških atoma, naučnici su bili u stanju da odrede fazni ugao.
Ipak postojao je još jedan problem. Pošto su ribozomi jako veliki i puno se teških atoma veže za njih, bilo je teško odmah odrediti fazni ugao. Bilo je potrebno još informacija da bi se rešio fazni problem.
Upravo je Tomas Steic bio taj koji je rešio zadatak. On je koristio slike ribozoma Joakima Franka (Joachim Frank), specijaliste za elektronsku mikroskopiju. Uz pomoć tih slika, Tomas je bio u mogućnosti da sazna kako su ribozomi orijentisani i locirani u kristalu (ali rezolucija mu nije omogućila da vidi atome ponaosob). Ova infromacija, zajedno sa informacijom od tepkih atoma, konačno je rešila fazni problem.
Zaključci nakon 20 godina rada
1998. godine, Tomas Steic je objavio prvu kristalnu strukturu ribozomske velike podjedinice. Ona je ličila na mutnu fotografiju i imala je rezoluciju od 9 angstrema (1 angstrem jednak je 10^10 metara). Nije bilo moguće videti odvojeno atome, ali mogli su se uočiti ribozomski dugački RNK molekuli. Ovo je predstavljalo veliki proboj.
Sada kada je fazni problem bio konačno rešen, ono što je preostalo bilo je poboljšavanje kristala i sakupljanje još podataka, kako bi se povećala oštrina slike. Ovogodišnji dobitnici Nobelove nagrade došli su do rešenja gotovo istovremeno. U avgustu i septembru 2000. godine, oni su objavili kristalne strukture sa rezolucijama koje su omogućavale interpretaciju atomskih položaja. Tomas Steic je dobio strukturu velike podjedinice ribozoma mikroorganizma Haloarcula marismortui, a Ada Jonat i Venkartraman Ramakrišnan su uspeli da dobiju strukturu male podjedinice ribozoma bakterije Thermus thermophilus. Stoga, bilo je moguće mapirati funkcije ribozoma na najosnovnijem - atomskom nivou.
Dupla kontrola male podjedinice
Svojstvo ribozoma koje je fasciniralo naučnike tokom dugog vremena jeste retkost grešaka tokom prevođenja DNK/RNK jezika u proteinski jezik. Ako je amino kiselina pogrešno ugrađena, protein može potpuno izgubiti svoju funkciju ili još gore, započeti da funkcioniše pogrešno.
Izbor prave amino kiseline zavisi najviše od osnovnih parova koji se formiraju između tRNK i iRNK. Međutim, ovaj proces uparivanja nije dovoljan da bi objasnio preciznost ribozoma.
Kristalne strukture male podjedinice ribozoma koje je dobio Venkatraman Ramakrišnan bile su presudne za razumevanje preciznosti koju ribozom postiže. On je uvideo nešto što se može opisati kao molekularni lenjir. Nukleotidi u maloj podjedinici rRNK mere udaljenost između kodona u iRNK i antikodona u tRNK. Ako je udaljenost netačna, molekul tRNK otpada sa ribozoma. Koristeći lenjir dvaput, ribozom vrši duplu proveru da je sve u redu. To omogućuje da se greške pojavljuju tek oko jednom na 100 000 amino kiselina.
Velika podjedinica niže kuglice
Uloga velike podjedinice u ribozomu je pre svega sinteza novog proteina. Ona aktivira formaciju peptidnih veza između amino kiselina. Dobijanje slike ove hemijske reakcije u koracima je veoma teško, pošto se događa na atomskom nivou pri ogromnoj brzini. U jednom ribozomu se može formirati oko 20 peptidnih veza svake sekunde.
Tomas Steic je međutim uspeo da zamrzne određene trenutke ove hemijske reakcije. On je kristalizovao veliku podjedinicu sa moleukilma koji liče na one koji su umešani u formiranje peptidnih veza. Uz pomoć ovih struktura, naučnici su bili u stanju da otkriju koji atomi ribozoma su važni za reakciju i kako se reakcija odvija.
Dobitnici Nobelove nagrade iz hemije 2009. godine, skovali su razumevanje koje na atomskom nivou objašnjava kako priroda može transformisati nešto tako prosto kao što je kod od 4 znaka u nešto tako komplikovano poput samog života, baš kao što je Džejms Votson predvideo 1964. godine. Istraživanje vođeno radoznalošću, kao što to često biva, može biti i od praktičnog značaja. Ovog puta, pokazalo se da se poznavanje strukture ribozoma može iskoristiti u potrazi za novim antibioticima.
Ribozom – meta za nove antibiotike
 Danas, ljudi imaju čitav arsenal različitih antibiotika koji se mogu koristiti u borbi protiv patoloških bakterija. Mnogi od tih antibiotika ubijaju bakterije blokirajući funkcije njihovih ribozoma. Međutim, bakterije su postale otporne na ove lekove u pretećoj meri. Zato su nam potrebni novi.
Danas, ljudi imaju čitav arsenal različitih antibiotika koji se mogu koristiti u borbi protiv patoloških bakterija. Mnogi od tih antibiotika ubijaju bakterije blokirajući funkcije njihovih ribozoma. Međutim, bakterije su postale otporne na ove lekove u pretećoj meri. Zato su nam potrebni novi. Ovogodišnji dobitnici Nobelove nagrade iz hemije su pronašli strukture koje pokazuju kako se različiti antibiotici vežu za ribozome. Neki od njih blokiraju tunel u kome rastući proteini napuštaju ribozome, drugi sprečavaju formiranje peptidne veze između amino kiselina, dok neki treći kvare prevod sa DNK/RNK jezika na proteinski jezik.
Nekoliko farmaceutskih kompanija sada koristi strukturu ribozoma kako bi razvili nove antibiotike. Neke od njih trenutno podležu kliničkim testovima u cilju da se uhvate u koštac sa problemom multirezistantnih bakterija.
Razumevanje strukture ribozoma, kao i same njihove funkcije, od velikog je značaja za čovečanstvo. Otkrića Ade Jonat, Tomasa Steica i Venkatramana Ramakrišnana su važna koliko za razumevanje kako sami životni procesi funkcionišu, toliko i za spašavanje života.
